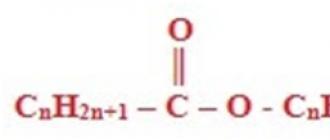हालाँकि, यह ध्यान देने योग्य है कि उनके उपयोग का मानव शरीर पर बहुत बड़ा सकारात्मक प्रभाव पड़ता है, और कार्बोहाइड्रेट और प्रोटीन की तरह ही उपभोग के लिए आवश्यक है।
ये एस्टर क्या हैं?
एस्टर, या एस्टर, जैसा कि उन्हें भी कहा जाता है, ऑक्सोएसिड (कार्बन, साथ ही अकार्बनिक यौगिक) के व्युत्पन्न हैं जिनका एक सामान्य सूत्र है, और, वास्तव में, ऐसे उत्पाद हैं जो हाइड्रॉक्सिल के हाइड्रोजन परमाणुओं को बदलते हैं - OH एक अम्लीय कार्य के साथ एक हाइड्रोकार्बन अवशेष (एलिफ़ैटिक, एल्केनाइल, एरोमैटिक या हेटेरोएरोमैटिक), उन्हें अल्कोहल के एसाइल डेरिवेटिव के रूप में भी माना जाता है।
सबसे आम एस्टर और उनके अनुप्रयोग के क्षेत्र
- एसीटेट एसिटिक एसिड के एस्टर हैं जिनका उपयोग विलायक के रूप में किया जाता है।
- लैक्टेट लैक्टिक एसिड होते हैं और इनका कार्बनिक उपयोग होता है।
- ब्यूटिरेट्स तैलीय होते हैं और इनका जैविक उपयोग भी होता है।
- फॉर्मेट्स फॉर्मिक एसिड होते हैं, लेकिन उनकी उच्च विष क्षमता के कारण, उनका विशेष रूप से उपयोग नहीं किया जाता है।
- यह आइसोबुटिल अल्कोहल, साथ ही सिंथेटिक फैटी एसिड और एल्केलीन कार्बोनेट पर आधारित सॉल्वैंट्स का भी उल्लेख करने योग्य है।
- मिथाइल एसीटेट - इसका उत्पादन लकड़ी के अल्कोहल घोल के रूप में किया जाता है। पॉलीविनाइल अल्कोहल के उत्पादन के दौरान, यह एक अतिरिक्त उत्पाद के रूप में बनता है। इसकी घुलने की क्षमता के कारण, इसका उपयोग एसीटोन के विकल्प के रूप में किया जाता है, लेकिन इसमें अधिक विषैले गुण होते हैं।
- एथिल एसीटेट - यह एस्टर सिंथेटिक और वन रासायनिक एसिटिक एसिड के प्रसंस्करण के दौरान वन रासायनिक उद्यमों में एस्टरीकरण विधि का उपयोग करके बनाया जाता है। आप मिथाइल अल्कोहल पर आधारित एथिल एसीटेट भी प्राप्त कर सकते हैं। एथिल एसीटेट में एसीटोन जैसे अधिकांश पॉलिमर को घोलने की क्षमता होती है। यदि आवश्यक हो, तो आप कजाकिस्तान में एथिल एसीटेट खरीद सकते हैं। उनकी क्षमताएं महान हैं. इस प्रकार, एसीटोन की तुलना में इसका लाभ यह है कि इसका क्वथनांक काफी अधिक होता है और अस्थिरता कम होती है। इसमें 15-20% एथिल अल्कोहल मिलाने लायक है और घुलने की क्षमता बढ़ जाती है।
- प्रोपाइल एसीटेट में एथिल एसीटेट के समान घुलनशील गुण होते हैं।
- एमाइल एसीटेट - इसकी सुगंध केले के तेल की गंध जैसी होती है। आवेदन का क्षेत्र - वार्निश विलायक, क्योंकि यह धीरे-धीरे घुल जाता है।
- फलों की सुगंध के साथ एस्टर.
- विनाइल एसीटेट - अनुप्रयोगों में चिपकने वाले, पेंट और रेजिन की तैयारी शामिल है।
- सोडियम और पोटैशियम लवण साबुन बनाते हैं।
एस्टर के फायदे और उपयोग के दायरे की थोड़ी जांच और अध्ययन करने के बाद, आप समझते हैं कि वे मानव जीवन में एक बड़ी आवश्यकता हैं। गतिविधि के कई क्षेत्रों में विकास में योगदान दें।
10.5. एस्टर। वसा
एस्टर- कार्बोक्जिलिक एसिड के कार्यात्मक व्युत्पन्न,
उन अणुओं में जिनमें हाइड्रॉक्सिल समूह (-OH) को अल्कोहल अवशेष (-) द्वारा प्रतिस्थापित किया जाता हैया)
कार्बोक्जिलिक एसिड के एस्टर - सामान्य सूत्र वाले यौगिक।
आर-कूअर", जहां R और R" हाइड्रोकार्बन रेडिकल हैं।
संतृप्त मोनोबैसिक कार्बोक्जिलिक एसिड के एस्टर एक सामान्य सूत्र है:

भौतिक गुण:
· अस्थिर, रंगहीन तरल पदार्थ
· पानी में खराब घुलनशील
· अक्सर सुखद गंध के साथ
पानी से भी हल्का
एस्टर फूलों, फलों और जामुनों में पाए जाते हैं। वे अपनी विशिष्ट गंध निर्धारित करते हैं।
वे आवश्यक तेलों का एक घटक हैं (लगभग 3000 ईएम ज्ञात हैं - नारंगी, लैवेंडर, गुलाब, आदि)
कम कार्बोक्जिलिक एसिड और कम मोनोहाइड्रिक अल्कोहल के एस्टर में फूलों, जामुन और फलों की सुखद गंध होती है। उच्च मोनोबैसिक एसिड और उच्च मोनोहाइड्रिक अल्कोहल के एस्टर प्राकृतिक वैक्स का आधार हैं। उदाहरण के लिए, मोम में पामिटिक एसिड और माय्रिसिल अल्कोहल (माइरिसिल पामिटेट) का एस्टर होता है:
सीएच 3 (सीएच 2) 14 -सीओ-ओ-(सीएच 2) 29 सीएच 3
सुगंध. संरचनात्मक सूत्र। |
एस्टर नाम |
सेब
|
इथाइल ईथर 2-मिथाइलबुटानोइक एसिड |
चेरी
|
एमाइल फॉर्मिक एसिड एस्टर |
नाशपाती
|
एसिटिक एसिड का आइसोमाइल एस्टर |
एक अनानास |
ब्यूटिरिक एसिड एथिल एस्टर (एथिल ब्यूटायरेट) |
केला |
एसिटिक एसिड का आइसोबुटिल एस्टर (आइसोमाइल एसीटेट में केले की गंध भी होती है) |
चमेली
|
बेंजाइल ईथर एसीटेट (बेंज़िल एसीटेट) |
एस्टर के संक्षिप्त नाम अल्कोहल अवशेषों में रेडिकल (आर") के नाम और एसिड अवशेषों में आरसीओओ समूह के नाम पर आधारित हैं। उदाहरण के लिए, एथिल एसिटिक एसिड सीएच 3 सीओओ सी 2 एच 5बुलाया एथिल एसीटेट.

आवेदन
· भोजन और इत्र (साबुन, इत्र, क्रीम का उत्पादन) उद्योगों में सुगंध और गंध बढ़ाने वाले के रूप में;
· प्लास्टिसाइज़र के रूप में प्लास्टिक और रबर के उत्पादन में।

प्लास्टिसाइज़र – वे पदार्थ जो प्रसंस्करण और संचालन के दौरान लोच और (या) प्लास्टिसिटी प्रदान करने (या बढ़ाने) के लिए बहुलक सामग्रियों की संरचना में पेश किए जाते हैं।
चिकित्सा में आवेदन
19वीं सदी के अंत और 20वीं सदी की शुरुआत में, जब कार्बनिक संश्लेषण अपना पहला कदम उठा रहा था, तो फार्माकोलॉजिस्ट द्वारा कई एस्टर को संश्लेषित और परीक्षण किया गया था। वे सैलोल, वैलिडोल आदि जैसी दवाओं का आधार बन गए। मिथाइल सैलिसिलेट का व्यापक रूप से स्थानीय उत्तेजक और एनाल्जेसिक के रूप में उपयोग किया जाता था, जिसे अब व्यावहारिक रूप से अधिक प्रभावी दवाओं द्वारा प्रतिस्थापित किया गया है।
एस्टर की तैयारी
अल्कोहल के साथ कार्बोक्जिलिक एसिड की प्रतिक्रिया करके एस्टर प्राप्त किया जा सकता है ( एस्टरीफिकेशन प्रतिक्रिया). उत्प्रेरक खनिज अम्ल हैं।
एसिड कटैलिसीस के तहत एस्टरीफिकेशन प्रतिक्रिया प्रतिवर्ती है। विपरीत प्रक्रिया - कार्बोक्जिलिक एसिड और अल्कोहल बनाने के लिए पानी की क्रिया के तहत एस्टर का टूटना - कहलाता है एस्टर हाइड्रोलिसिस.
RCOOR " + H2O ( एच +) ↔ RCOOH + R "ओह
क्षार की उपस्थिति में हाइड्रोलिसिस अपरिवर्तनीय है (क्योंकि परिणामस्वरूप नकारात्मक रूप से चार्ज किए गए कार्बोक्जलेट आयन आरसीओओ न्यूक्लियोफिलिक अभिकर्मक - अल्कोहल के साथ प्रतिक्रिया नहीं करता है)।
इस प्रतिक्रिया को कहा जाता है एस्टर का साबुनीकरण(साबुन का उत्पादन करते समय वसा में एस्टर बांड के क्षारीय हाइड्रोलिसिस के अनुरूप)।
वसा, उनकी संरचना, गुण और अनुप्रयोग
"रसायन विज्ञान हर जगह है, रसायन शास्त्र हर चीज में है:
हर चीज़ में हम सांस लेते हैं
हम हर चीज़ में पीते हैं
हम जो कुछ भी खाते हैं उसमें।"
हम जो कुछ भी पहनते हैं उसमें



लोगों ने लंबे समय से प्राकृतिक वस्तुओं से वसा निकालना और रोजमर्रा की जिंदगी में इसका उपयोग करना सीखा है। आदिम दीपकों में वसा जलाई जाती थी, जिससे आदिम लोगों की गुफाएँ रोशन होती थीं; जिन धावकों पर जहाज चलाए जाते थे, उन्हें वसा से चिकना किया जाता था। वसा हमारे पोषण का मुख्य स्रोत हैं। लेकिन खराब पोषण और गतिहीन जीवनशैली के कारण वजन बढ़ जाता है। रेगिस्तानी जानवर ऊर्जा और पानी के स्रोत के रूप में वसा का भंडारण करते हैं। सील और व्हेल की मोटी वसा की परत उन्हें आर्कटिक महासागर के ठंडे पानी में तैरने में मदद करती है।
वसा प्रकृति में व्यापक रूप से वितरित होती है। कार्बोहाइड्रेट और प्रोटीन के साथ, वे सभी जानवरों और पौधों के जीवों का हिस्सा हैं और हमारे भोजन के मुख्य भागों में से एक हैं। वसा के स्रोत जीवित जीव हैं। जानवरों में गाय, सूअर, भेड़, मुर्गियां, सील, व्हेल, हंस, मछली (शार्क, कॉड, हेरिंग) शामिल हैं। मछली का तेल, एक औषधीय उत्पाद, कॉड और शार्क के जिगर से प्राप्त किया जाता है, और खेत जानवरों को खिलाने के लिए उपयोग की जाने वाली वसा हेरिंग से प्राप्त की जाती है। वनस्पति वसा प्रायः तरल होती हैं और उन्हें तेल कहा जाता है। कपास, सन, सोयाबीन, मूंगफली, तिल, रेपसीड, सूरजमुखी, सरसों, मक्का, खसखस, भांग, नारियल, समुद्री हिरन का सींग, गुलाब कूल्हों, ताड़ के तेल और कई अन्य पौधों से प्राप्त वसा का उपयोग किया जाता है।

वसा विभिन्न कार्य करते हैं: निर्माण, ऊर्जा (1 ग्राम वसा 9 किलो कैलोरी ऊर्जा प्रदान करता है), सुरक्षात्मक, भंडारण। वसा किसी व्यक्ति के लिए आवश्यक ऊर्जा का 50% प्रदान करती है, इसलिए एक व्यक्ति को प्रतिदिन 70-80 ग्राम वसा का उपभोग करने की आवश्यकता होती है। एक स्वस्थ व्यक्ति के शरीर के वजन का 10-20% वसा होता है। वसा फैटी एसिड का एक आवश्यक स्रोत हैं। कुछ वसा में विटामिन ए, डी, ई, के और हार्मोन होते हैं।
कई जानवर और मनुष्य वसा का उपयोग गर्मी-इन्सुलेटिंग शेल के रूप में करते हैं; उदाहरण के लिए, कुछ समुद्री जानवरों में वसा परत की मोटाई एक मीटर तक पहुंच जाती है। इसके अलावा, वसा शरीर में स्वाद बढ़ाने वाले एजेंटों और रंगों के लिए विलायक हैं। कई विटामिन, जैसे विटामिन ए, केवल वसा में घुलनशील होते हैं।
कुछ जानवर (आमतौर पर जलपक्षी) अपने स्वयं के मांसपेशी फाइबर को चिकनाई देने के लिए वसा का उपयोग करते हैं।
वसा खाद्य पदार्थों के तृप्ति प्रभाव को बढ़ाती है क्योंकि वे बहुत धीरे-धीरे पचते हैं और भूख लगने में देरी करते हैं। .
वसा की खोज का इतिहास
17वीं शताब्दी में वापस। जर्मन वैज्ञानिक, पहले विश्लेषणात्मक रसायनज्ञों में से एक ओटो टैचेनी(1652-1699) ने सबसे पहले सुझाव दिया कि वसा में "छिपा हुआ एसिड" होता है।
1741 में फ्रांसीसी रसायनज्ञ क्लाउड जोसेफ जियोफ़रॉय(1685-1752) ने पाया कि जब साबुन (जो वसा को क्षार के साथ उबालकर तैयार किया गया था) एसिड के साथ विघटित होता है, तो एक द्रव्यमान बनता है जो छूने पर चिकना होता है।
यह तथ्य कि वसा और तेल में ग्लिसरीन होता है, सबसे पहले 1779 में प्रसिद्ध स्वीडिश रसायनज्ञ द्वारा खोजा गया था कार्ल विल्हेम शीले।
वसा की रासायनिक संरचना पहली बार पिछली शताब्दी की शुरुआत में एक फ्रांसीसी रसायनज्ञ द्वारा निर्धारित की गई थी। मिशेल यूजीन शेवरूल, वसा के रसायन विज्ञान के संस्थापक, उनकी प्रकृति के कई अध्ययनों के लेखक, छह-खंड मोनोग्राफ "पशु उत्पत्ति के निकायों के रासायनिक अध्ययन" में संक्षेपित हैं।
1813 ई. शेवरूल क्षारीय वातावरण में वसा की हाइड्रोलिसिस प्रतिक्रिया के कारण, वसा की संरचना स्थापित की गई। उन्होंने दिखाया कि वसा में ग्लिसरॉल और फैटी एसिड होते हैं, और यह सिर्फ उनका मिश्रण नहीं है, बल्कि एक यौगिक है, जो पानी जोड़ने पर टूट जाता है ग्लिसरॉल और एसिड में.
वसा संश्लेषण

1854 में, फ्रांसीसी रसायनज्ञ मार्सेलिन बर्थेलॉट (1827-1907) ने एस्टरीफिकेशन प्रतिक्रिया को अंजाम दिया, यानी ग्लिसरॉल और फैटी एसिड के बीच एस्टर का निर्माण, और इस तरह पहली बार वसा का संश्लेषण किया।

वसा का सामान्य सूत्र (ट्राइग्लिसराइड्स)

वसा
- ग्लिसरॉल के एस्टर और उच्च कार्बोक्जिलिक एसिड।
इन यौगिकों का सामान्य नाम ट्राइग्लिसराइड्स है।
वसा का वर्गीकरण



पशु वसा में मुख्य रूप से संतृप्त एसिड के ग्लिसराइड होते हैं और ये ठोस होते हैं। वनस्पति वसा, जिन्हें अक्सर तेल कहा जाता है, में असंतृप्त कार्बोक्जिलिक एसिड के ग्लिसराइड होते हैं। ये हैं, उदाहरण के लिए, तरल सूरजमुखी, भांग और अलसी के तेल।

प्राकृतिक वसा में निम्नलिखित फैटी एसिड होते हैं
संतृप्त: स्टीयरिक (सी 17 एच 35 सीओओएच) पामिटिक (सी 15 एच 31 सीओओएच) तैलीय (C 3 H 7 COOH) |
युक्त जानवरों वसा |
असंतृप्त : ओलिक (सी 17 एच 33 सीओओएच, 1 दोहरा बंधन) लिनोलिक (सी 17 एच 31 सीओओएच, 2 दोहरे बंधन) लिनोलेनिक (सी 17 एच 29 सीओओएच, 3 दोहरे बंधन) एराकिडोनिक (सी 19 एच 31 सीओओएच, 4 दोहरे बंधन, कम आम) |
युक्त पौधा वसा |
वसा सभी पौधों और जानवरों में पाई जाती है। वे पूर्ण ग्लिसरॉल एस्टर के मिश्रण हैं और उनमें स्पष्ट रूप से परिभाषित गलनांक नहीं होता है।
· पशु वसा(भेड़ का बच्चा, सूअर का मांस, गोमांस, आदि), एक नियम के रूप में, कम पिघलने बिंदु वाले ठोस पदार्थ होते हैं (मछली का तेल एक अपवाद है)। ठोस वसा में अवशेषों की प्रधानता होती है तर-बतरअम्ल
· वनस्पति वसा - तेल (सूरजमुखी, सोयाबीन, बिनौला, आदि) - तरल पदार्थ (अपवाद - नारियल तेल, कोकोआ बीन मक्खन)। तेलों में मुख्यतः अवशेष होते हैं असंतृप्त (असंतृप्त)अम्ल
वसा के रासायनिक गुण
1. हाइड्रोलिसिस,या सैपोनिफिकेशन , मोटा पानी के प्रभाव में होता है, एंजाइम या एसिड उत्प्रेरक (प्रतिवर्ती) की भागीदारी के साथ, इस मामले में, अल्कोहल - ग्लिसरीन और कार्बोक्जिलिक एसिड का मिश्रण बनता है:

या क्षार (अपरिवर्तनीय). क्षारीय हाइड्रोलिसिस से उच्च फैटी एसिड के लवण उत्पन्न होते हैं, जिन्हें साबुन कहा जाता है। साबुन क्षार की उपस्थिति में वसा के जल अपघटन द्वारा प्राप्त किये जाते हैं:

साबुन उच्च कार्बोक्जिलिक एसिड के पोटेशियम और सोडियम लवण हैं।
2. वसा का हाइड्रोजनीकरण – खाद्य प्रयोजनों के लिए तरल वनस्पति तेलों को ठोस वसा में बदलना बहुत महत्वपूर्ण है। तेल हाइड्रोजनीकरण का उत्पाद ठोस वसा (कृत्रिम चरबी, सैलोमास). नकली मक्खन- खाद्य वसा में हाइड्रोजनीकृत तेल (सूरजमुखी, मक्का, बिनौला, आदि), पशु वसा, दूध और स्वाद देने वाले योजक (नमक, चीनी, विटामिन, आदि) का मिश्रण होता है।
उद्योग में मार्जरीन का उत्पादन इस प्रकार किया जाता है:

तेल हाइड्रोजनीकरण प्रक्रिया (उच्च तापमान, धातु उत्प्रेरक) की शर्तों के तहत, सीआईएस सी = सी बांड वाले कुछ एसिड अवशेषों को अधिक स्थिर ट्रांस आइसोमर्स में आइसोमेराइज किया जाता है। मार्जरीन (विशेष रूप से सस्ती किस्मों में) में ट्रांस-असंतृप्त एसिड अवशेषों की बढ़ी हुई सामग्री एथेरोस्क्लेरोसिस, हृदय और अन्य बीमारियों का खतरा बढ़ाती है।

वसा उत्पादन प्रतिक्रिया (एस्टरीफिकेशन)

वसा का प्रयोग


वसा एक खाद्य उत्पाद है। वसा की जैविक भूमिका
पशु वसा और वनस्पति तेल, प्रोटीन और कार्बोहाइड्रेट के साथ, सामान्य मानव पोषण के मुख्य घटकों में से एक हैं। वे ऊर्जा का मुख्य स्रोत हैं: 1 ग्राम वसा, जब पूरी तरह से ऑक्सीकरण होता है (यह ऑक्सीजन की भागीदारी के साथ कोशिकाओं में होता है), 9.5 kcal (लगभग 40 kJ) ऊर्जा प्रदान करता है, जो कि प्राप्त की जा सकने वाली ऊर्जा से लगभग दोगुनी है। प्रोटीन या कार्बोहाइड्रेट. इसके अलावा, शरीर में वसा भंडार में व्यावहारिक रूप से कोई पानी नहीं होता है, जबकि प्रोटीन और कार्बोहाइड्रेट अणु हमेशा पानी के अणुओं से घिरे रहते हैं। परिणामस्वरूप, एक ग्राम वसा एक ग्राम पशु स्टार्च - ग्लाइकोजन की तुलना में लगभग 6 गुना अधिक ऊर्जा प्रदान करता है। इस प्रकार, वसा को उचित रूप से उच्च-कैलोरी "ईंधन" माना जाना चाहिए। यह मुख्य रूप से मानव शरीर के सामान्य तापमान को बनाए रखने के साथ-साथ विभिन्न मांसपेशियों को काम करने के लिए खर्च किया जाता है, इसलिए जब कोई व्यक्ति कुछ भी नहीं कर रहा होता है (उदाहरण के लिए, सो रहा है), तो उसे ऊर्जा लागत को कवर करने के लिए हर घंटे लगभग 350 kJ ऊर्जा की आवश्यकता होती है। , लगभग एक विद्युत 100-वाट प्रकाश बल्ब के समान शक्ति।
प्रतिकूल परिस्थितियों में शरीर को ऊर्जा प्रदान करने के लिए, इसमें वसा का भंडार बनाया जाता है, जो चमड़े के नीचे के ऊतकों में, पेरिटोनियम की वसायुक्त तह में - तथाकथित ओमेंटम में जमा हो जाता है। चमड़े के नीचे की वसा शरीर को हाइपोथर्मिया से बचाती है (वसा का यह कार्य समुद्री जानवरों के लिए विशेष रूप से महत्वपूर्ण है)। हजारों वर्षों से, लोगों ने कठिन शारीरिक श्रम किया है, जिसके लिए बड़ी मात्रा में ऊर्जा की आवश्यकता होती है और, तदनुसार, पोषण में वृद्धि होती है। किसी व्यक्ति की न्यूनतम दैनिक ऊर्जा आवश्यकता को पूरा करने के लिए केवल 50 ग्राम वसा ही पर्याप्त है। हालाँकि, मध्यम शारीरिक गतिविधि के साथ, एक वयस्क को भोजन से थोड़ा अधिक वसा प्राप्त करना चाहिए, लेकिन उनकी मात्रा 100 ग्राम से अधिक नहीं होनी चाहिए (यह लगभग 3000 किलो कैलोरी के आहार के लिए कैलोरी सामग्री का एक तिहाई प्रदान करता है)। यह ध्यान दिया जाना चाहिए कि इन 100 ग्राम में से आधे तथाकथित छिपे हुए वसा के रूप में भोजन में निहित हैं। वसा लगभग सभी खाद्य उत्पादों में पाए जाते हैं: वे आलू (0.4%), ब्रेड (1-2%), और दलिया (6%) में भी थोड़ी मात्रा में पाए जाते हैं। दूध में आमतौर पर 2-3% वसा होती है (लेकिन मलाई रहित दूध की विशेष किस्में भी होती हैं)। दुबले मांस में काफी मात्रा में छिपी हुई वसा होती है - 2 से 33% तक। उत्पाद में छिपी हुई वसा अलग-अलग छोटे कणों के रूप में मौजूद होती है। लगभग शुद्ध वसा चरबी और वनस्पति तेल हैं; मक्खन में लगभग 80% वसा होती है, और घी में 98% वसा होती है। बेशक, वसा की खपत के लिए दी गई सभी सिफारिशें औसत हैं; वे लिंग और उम्र, शारीरिक गतिविधि और जलवायु परिस्थितियों पर निर्भर करती हैं। वसा के अत्यधिक सेवन से व्यक्ति का वजन तेजी से बढ़ता है, लेकिन हमें यह नहीं भूलना चाहिए कि शरीर में वसा अन्य खाद्य पदार्थों से भी संश्लेषित हो सकती है। शारीरिक गतिविधि के माध्यम से अतिरिक्त कैलोरी कम करना इतना आसान नहीं है। उदाहरण के लिए, 7 किमी की जॉगिंग के बाद, एक व्यक्ति लगभग उतनी ही ऊर्जा खर्च करता है जितनी वह सिर्फ एक सौ ग्राम चॉकलेट बार (35% वसा, 55% कार्बोहाइड्रेट) खाने से प्राप्त करता है। फिजियोलॉजिस्ट ने पाया है कि शारीरिक गतिविधि के साथ यह 10 गुना अधिक है सामान्य से अधिक, वसायुक्त आहार प्राप्त करने वाला व्यक्ति 1.5 घंटे के बाद पूरी तरह से थक गया था। कार्बोहाइड्रेट आहार के साथ, एक व्यक्ति 4 घंटे तक समान भार झेलता है। यह प्रतीत होता है कि विरोधाभासी परिणाम जैव रासायनिक प्रक्रियाओं की विशिष्टताओं द्वारा समझाया गया है। वसा की उच्च "ऊर्जा तीव्रता" के बावजूद, शरीर में उनसे ऊर्जा प्राप्त करना एक धीमी प्रक्रिया है। यह वसा की कम प्रतिक्रियाशीलता के कारण है, विशेषकर उनकी हाइड्रोकार्बन श्रृंखलाओं के कारण। कार्बोहाइड्रेट, हालांकि वे वसा की तुलना में कम ऊर्जा प्रदान करते हैं, इसे बहुत तेजी से "रिलीज़" करते हैं। इसलिए, शारीरिक गतिविधि से पहले, वसायुक्त खाद्य पदार्थों के बजाय मिठाई खाना बेहतर है। भोजन में वसा की अधिकता, विशेष रूप से जानवरों में, एथेरोस्क्लेरोसिस, हृदय विफलता आदि जैसी बीमारियों के विकसित होने का खतरा बढ़ जाता है। पशु वसा में बहुत अधिक कोलेस्ट्रॉल होता है ( लेकिन हमें यह नहीं भूलना चाहिए कि दो-तिहाई कोलेस्ट्रॉल शरीर में कम वसा वाले खाद्य पदार्थों - कार्बोहाइड्रेट और प्रोटीन) से संश्लेषित होता है।
यह ज्ञात है कि उपभोग की जाने वाली वसा का एक महत्वपूर्ण हिस्सा वनस्पति तेल होना चाहिए, जिसमें ऐसे यौगिक होते हैं जो शरीर के लिए बहुत महत्वपूर्ण होते हैं - कई दोहरे बंधन वाले पॉलीअनसेचुरेटेड फैटी एसिड। इन अम्लों को "आवश्यक" कहा जाता है। विटामिन की तरह, उन्हें तैयार रूप में शरीर में प्रवेश करना चाहिए। इनमें से एराकिडोनिक एसिड में सबसे अधिक गतिविधि होती है (यह शरीर में लिनोलिक एसिड से संश्लेषित होता है), और लिनोलेनिक एसिड में सबसे कम गतिविधि होती है (लिनोलेनिक एसिड से 10 गुना कम)। विभिन्न अनुमानों के अनुसार, एक व्यक्ति की लिनोलिक एसिड की दैनिक आवश्यकता 4 से 10 ग्राम तक होती है। लिनोलिक एसिड की सबसे अधिक मात्रा (84% तक) कुसुम तेल में होती है, जो कुसुम के बीज से निचोड़ा जाता है, जो चमकीले नारंगी फूलों वाला एक वार्षिक पौधा है। . सूरजमुखी और अखरोट के तेल में भी यह एसिड काफी मात्रा में होता है।
पोषण विशेषज्ञों के अनुसार, संतुलित आहार में 10% पॉलीअनसेचुरेटेड एसिड, 60% मोनोअनसेचुरेटेड एसिड (मुख्य रूप से ओलिक एसिड) और 30% संतृप्त एसिड होना चाहिए। यह वह अनुपात है जो सुनिश्चित किया जाता है यदि किसी व्यक्ति को तरल वनस्पति तेलों के रूप में एक तिहाई वसा प्राप्त होती है - प्रति दिन 30-35 ग्राम की मात्रा में। मार्जरीन में ये तेल भी शामिल हैं, जिनमें 15 से 22% संतृप्त फैटी एसिड, 27 से 49% असंतृप्त और 30 से 54% पॉलीअनसेचुरेटेड होते हैं। तुलना के लिए: मक्खन में 45-50% संतृप्त फैटी एसिड, 22-27% असंतृप्त और 1% से कम पॉलीअनसेचुरेटेड होता है। इस संबंध में, उच्च गुणवत्ता वाला मार्जरीन मक्खन की तुलना में स्वास्थ्यवर्धक है।
याद रखना चाहिए!!!
संतृप्त फैटी एसिड वसा चयापचय, यकृत समारोह को नकारात्मक रूप से प्रभावित करते हैं और एथेरोस्क्लेरोसिस के विकास में योगदान करते हैं। असंतृप्त एसिड (विशेषकर लिनोलिक और एराकिडोनिक एसिड) वसा चयापचय को नियंत्रित करते हैं और शरीर से कोलेस्ट्रॉल को हटाने में भाग लेते हैं। असंतृप्त वसीय अम्लों की मात्रा जितनी अधिक होगी, वसा का गलनांक उतना ही कम होगा। ठोस पशु वसा और तरल वनस्पति वसा की कैलोरी सामग्री लगभग समान है, लेकिन वनस्पति वसा का शारीरिक मूल्य बहुत अधिक है। दूध की वसा में अधिक मूल्यवान गुण होते हैं। इसमें एक तिहाई असंतृप्त वसा अम्ल होते हैं और इमल्शन के रूप में संरक्षित होने पर यह शरीर द्वारा आसानी से अवशोषित हो जाता है। इन सकारात्मक गुणों के बावजूद, आपको केवल दूध वसा का सेवन नहीं करना चाहिए, क्योंकि किसी भी वसा में फैटी एसिड की आदर्श संरचना नहीं होती है। पशु और पौधे दोनों मूल की वसा का सेवन करना सबसे अच्छा है। युवा लोगों और मध्यम आयु वर्ग के लोगों के लिए उनका अनुपात 1:2.3 (70% पशु और 30% पौधा) होना चाहिए। वृद्ध लोगों के आहार में वनस्पति वसा की प्रधानता होनी चाहिए।
वसा न केवल चयापचय प्रक्रियाओं में भाग लेते हैं, बल्कि आरक्षित रूप में भी संग्रहीत होते हैं (मुख्य रूप से पेट की दीवार और गुर्दे के आसपास)। वसा भंडार चयापचय प्रक्रियाएं प्रदान करते हैं, जीवन के लिए प्रोटीन को संरक्षित करते हैं। यह वसा शारीरिक गतिविधि के दौरान ऊर्जा प्रदान करती है, यदि भोजन के साथ कम वसा की आपूर्ति की जाती है, साथ ही गंभीर बीमारियों के दौरान, जब भूख कम होने के कारण भोजन के साथ इसकी पर्याप्त आपूर्ति नहीं हो पाती है।
भोजन में वसा का अत्यधिक सेवन स्वास्थ्य के लिए हानिकारक है: यह बड़ी मात्रा में रिजर्व में जमा हो जाता है, जिससे शरीर का वजन बढ़ जाता है, जिससे कभी-कभी आकृति ख़राब हो जाती है। रक्त में इसकी सांद्रता बढ़ जाती है, जो जोखिम कारक के रूप में एथेरोस्क्लेरोसिस, कोरोनरी हृदय रोग, उच्च रक्तचाप आदि के विकास में योगदान देता है।
अभ्यास
1. एक ही संरचना के दो कार्बनिक यौगिकों का मिश्रण 148 ग्राम है: सी 3 एच 6 ओ 2। इन सोयाबीन की संरचना निर्धारित करें मिश्रण में डायेनियम और उनके द्रव्यमान अंश, यदि यह ज्ञात हो कि इनमें से एकअतिरिक्त सोडियम बाइकार्बोनेट के साथ बातचीत करते समय, वे 22.4 लीटर (एनएस) कार्बन मोनोऑक्साइड छोड़ते हैं ( चतुर्थ), और दूसरा सोडियम कार्बोनेट और सिल्वर ऑक्साइड के अमोनिया घोल के साथ प्रतिक्रिया नहीं करता है, लेकिन जब सोडियम हाइड्रॉक्साइड के जलीय घोल के साथ गर्म किया जाता है तो यह अल्कोहल और एसिड नमक बनाता है।
समाधान:
यह ज्ञात है कि कार्बन मोनोऑक्साइड (चतुर्थ ) तब निकलता है जब सोडियम कार्बोनेट किसी अम्ल के साथ प्रतिक्रिया करता है। संरचना C 3 H 6 O 2 का केवल एक एसिड हो सकता है - प्रोपियोनिक, CH 3 CH 2 COOH।
C 2 H 5 COOH + N aHCO 3 → C 2 H 5 COONa + CO 2 + H 2 O।
शर्त के मुताबिक 22.4 लीटर CO 2 निकली, यानी 1 mol, यानी मिश्रण में 1 mol एसिड भी था. प्रारंभिक कार्बनिक यौगिकों का दाढ़ द्रव्यमान है:एम (सी 3 एच 6 ओ 2) = 74 ग्राम/मोल, इसलिए 148 ग्राम 2 मोल है।
हाइड्रोलिसिस पर दूसरा यौगिक एक अल्कोहल और एक एसिड नमक बनाता है, जिसका अर्थ है कि यह एक एस्टर है:
RCOOR' + NaOH → RCOONa + R'OH।
C 3 H 6 O 2 की संरचना दो एस्टर से मेल खाती है: एथिल फॉर्मेट HCOOC 2 H 5 और मिथाइल एसीटेट CH 3 COOCH 3। फॉर्मिक एसिड के एस्टर सिल्वर ऑक्साइड के अमोनिया घोल के साथ प्रतिक्रिया करते हैं, इसलिए पहला एस्टर समस्या की शर्तों को पूरा नहीं करता है। अतः मिश्रण में दूसरा पदार्थ मिथाइल एसीटेट है।
चूंकि मिश्रण में समान दाढ़ द्रव्यमान वाले यौगिकों का एक मोल होता है, इसलिए उनके द्रव्यमान अंश बराबर होते हैं और मात्रा 50% होती है।
उत्तर। 50% सीएच 3 सीएच 2 कूह, 50% सीएच 3 कूच 3।
2. हाइड्रोजन के संबंध में एस्टर वाष्प का सापेक्ष घनत्व 44 है। इस एस्टर के हाइड्रोलिसिस के दौरान, दो यौगिक बनते हैं, जिनके समान मात्रा में दहन करने पर समान मात्रा में कार्बन डाइऑक्साइड बनता है (समान परिस्थितियों में)। इस एस्टर का संरचनात्मक सूत्र.
समाधान:
संतृप्त अल्कोहल और एसिड द्वारा निर्मित एस्टर का सामान्य सूत्र C हैएन एन 2 एन ओ 2. n का मान हाइड्रोजन घनत्व से निर्धारित किया जा सकता है:
एम (सी एन एच 2 एन ओ 2) = 14 एन + 32 = 44. 2 = 88 ग्राम/मोल,
कहाँ से एन = 4, अर्थात् ईथर में 4 कार्बन परमाणु होते हैं। चूंकि एस्टर के हाइड्रोलिसिस के दौरान बनने वाले अल्कोहल और एसिड के दहन से समान मात्रा में कार्बन डाइऑक्साइड निकलता है, इसलिए एसिड और अल्कोहल में समान संख्या में कार्बन परमाणु होते हैं, प्रत्येक में दो। इस प्रकार, वांछित एस्टर एसिटिक एसिड और इथेनॉल द्वारा बनता है और इसे एथिल एसीटेट कहा जाता है:
सीएच 3 - |
ओ-एस 2 एन 5 |
उत्तर। एथिल एसीटेट, सीएच 3 एसओओसी 2 एच 5।
________________________________________________________________
3. एक एस्टर के हाइड्रोलिसिस के दौरान, जिसका दाढ़ द्रव्यमान 130 ग्राम/मोल है, एसिड ए और अल्कोहल बी बनते हैं। एस्टर की संरचना निर्धारित करें यदि यह ज्ञात हो कि एसिड के सिल्वर नमक में 59.66% सिल्वर होता है द्रव्यमान। अल्कोहल बी सोडियम डाइक्रोमेट द्वारा ऑक्सीकृत नहीं होता है और आसानी से हाइड्रोक्लोरिक एसिड के साथ प्रतिक्रिया करके एल्काइल क्लोराइड बनाता है।
समाधान:
एस्टर का सामान्य सूत्र होता है RCOOR '. यह ज्ञात है कि अम्ल का रजत नमक,आरसीओओएजी , में 59.66% चांदी होती है, इसलिए नमक का दाढ़ द्रव्यमान है:एम (आरसीओओएजी) = एम (ए जी )/0.5966 = 181 ग्राम/मोल, कहाँ सेश्री ) = 181-(12+2. 16+108) = 29 ग्राम/मोल। यह रेडिकल एथिल, सी 2 एच 5 है, और एस्टर का निर्माण प्रोपियोनिक एसिड द्वारा किया गया था:सी 2 एच 5 सीओओआर'।
दूसरे रेडिकल का दाढ़ द्रव्यमान है:एम (आर ') = एम (सी 2 एच 5 सीओओआर ') - एम(सी 2 एच 5 सीओओ) = 130-73 = 57 ग्राम/मोल। इस रेडिकल का आणविक सूत्र C 4 H 9 है। स्थिति के अनुसार, अल्कोहल C 4 H 9 OH ऑक्सीकरण नहीं करता हैना 2 सी र 2 O 7 और के साथ आसानी से प्रतिक्रिया करता हैएचसीएल इसलिए, यह अल्कोहल तृतीयक है, (CH 3) 3 SON।
इस प्रकार, वांछित एस्टर प्रोपियोनिक एसिड और टर्ट-ब्यूटेनॉल द्वारा बनता है और इसे टर्ट-ब्यूटाइलप्रोपियोनेट कहा जाता है:
सीएच 3 |
||
सी 2 एच 5 - |
सी—ओ— |
सी - सीएच 3 |
सीएच 3 |
उत्तर । टर्ट-ब्यूटाइल प्रोपियोनेट।
________________________________________________________________
4. वसा के लिए दो संभावित सूत्र लिखें, जिसके अणु में 57 कार्बन परमाणु होते हैं और 1:2 अनुपात में आयोडीन के साथ प्रतिक्रिया करते हैं। वसा में समान संख्या में कार्बन परमाणुओं के साथ एसिड अवशेष होते हैं।
समाधान:
वसा का सामान्य सूत्र:
जहां आर, आर', आर " - हाइड्रोकार्बन रेडिकल में विषम संख्या में कार्बन परमाणु होते हैं (अम्लीय अवशेषों से एक और परमाणु -CO- समूह का हिस्सा है)। तीन हाइड्रोकार्बन रेडिकल में 57-6 = 51 कार्बन परमाणु होते हैं। यह माना जा सकता है कि प्रत्येक रेडिकल इसमें 17 कार्बन परमाणु होते हैं।
चूँकि एक वसा अणु दो आयोडीन अणुओं को जोड़ सकता है, इसलिए प्रति तीन रेडिकल में दो दोहरे बंधन या एक ट्रिपल बंधन होते हैं। यदि दो दोहरे बंधन एक रेडिकल में हैं, तो वसा में लिनोलिक एसिड अवशेष होता है (आर = सी 17 एच 31) और दो स्टीयरिक एसिड अवशेष (आर' = आर " = सी 17 एच 35)। यदि दो दोहरे बंधन अलग-अलग रेडिकल में हैं, तो वसा में दो ओलिक एसिड अवशेष होते हैं (आर = आर ' = सी 17 एच 33 ) और एक स्टीयरिक एसिड अवशेष (आर " = सी 17 एच 35)। संभावित वसा सूत्र:
|
|
________________________________________________________________


5.

स्वतंत्र समाधान के लिए कार्य
1. एस्टरीफिकेशन प्रतिक्रिया क्या है?
2. ठोस और तरल वसा की संरचना में क्या अंतर है?
3. वसा के रासायनिक गुण क्या हैं?
4. मिथाइल फॉर्मेट के उत्पादन के लिए प्रतिक्रिया समीकरण दीजिए।
5. दो एस्टर और C 3 H 6 O 2 संरचना वाले एक एसिड के संरचनात्मक सूत्र लिखें। इन पदार्थों के नाम अंतर्राष्ट्रीय नामकरण के अनुसार बताइये।
6. एस्टरीफिकेशन प्रतिक्रियाओं के लिए समीकरण लिखें: ए) एसिटिक एसिड और 3-मिथाइलबुटानॉल-1; बी) ब्यूटिरिक एसिड और प्रोपेनॉल-1। ईथर का नाम बताएं.
7. यदि हाइड्रोलिसिस के परिणामस्वरूप बने एसिड को हाइड्रोजनीकृत करने के लिए 13.44 लीटर हाइड्रोजन (एन.एस.) की आवश्यकता होती है तो कितने ग्राम वसा ली गई थी?
8. यदि 24 ग्राम एस्टर बनता है, तो 32 ग्राम एसिटिक एसिड और 50 ग्राम 2-प्रोपेनॉल को सांद्र सल्फ्यूरिक एसिड की उपस्थिति में गर्म करने पर बनने वाले एस्टर की उपज के द्रव्यमान अंश की गणना करें।
9. 221 ग्राम वजन वाले वसा के नमूने को हाइड्रोलाइज करने के लिए 0.2 के क्षार द्रव्यमान अंश के साथ 150 ग्राम सोडियम हाइड्रॉक्साइड घोल की आवश्यकता थी। मूल वसा का संरचनात्मक सूत्र प्रस्तावित करें।
10. 0.25 के क्षार के द्रव्यमान अंश और 1.23 ग्राम/सेमी 3 के घनत्व के साथ पोटेशियम हाइड्रॉक्साइड के घोल की मात्रा की गणना करें, जिसे इथेनोइक एसिड एथिल एस्टर, मेथेनोइक एसिड से युक्त मिश्रण के 15 ग्राम के हाइड्रोलिसिस को पूरा करने के लिए उपभोग किया जाना चाहिए। प्रोपाइल एस्टर और प्रोपेनोइक एसिड मिथाइल एस्टर।
वीडियो अनुभव
1. एस्टर के उत्पादन का आधार कौन सी प्रतिक्रिया है: |
|
ए) निराकरण |
बी) पोलीमराइजेशन |
ग) एस्टरीफिकेशन |
घ) हाइड्रोजनीकरण |
2. कितने आइसोमेरिक एस्टर सूत्र C 4 H 8 O 2 के अनुरूप हैं: |
|
ए) 2 |
|
एस्टर के सबसे महत्वपूर्ण प्रतिनिधि वसा हैं।
वसा, तेल
वसा- ये ग्लिसरॉल और उच्चतर मोनोएटोमिक के एस्टर हैं। ऐसे यौगिकों का सामान्य नाम ट्राइग्लिसराइड्स या ट्राईसिलग्लिसरॉल्स है, जहां एसाइल एक कार्बोक्जिलिक एसिड अवशेष -सी(ओ)आर है। प्राकृतिक ट्राइग्लिसराइड्स की संरचना में संतृप्त एसिड (पामिटिक C 15 H 31 COOH, स्टीयरिक C 17 H 35 COOH) और असंतृप्त (ओलिक C 17 H 33 COOH, लिनोलिक C 17 H 31 COOH) के अवशेष शामिल हैं। उच्च कार्बोक्जिलिक एसिड जो वसा का हिस्सा होते हैं, उनमें हमेशा कार्बन परमाणुओं की एक समान संख्या (सी 8 - सी 18) और एक अशाखित हाइड्रोकार्बन अवशेष होता है। प्राकृतिक वसा और तेल उच्च कार्बोक्जिलिक एसिड के ग्लिसराइड का मिश्रण होते हैं।
वसा की संरचना और संरचना को सामान्य सूत्र द्वारा दर्शाया जा सकता है:

एस्टरीफिकेशन- एस्टर के गठन की प्रतिक्रिया.

वसा की संरचना में विभिन्न संयोजनों में संतृप्त और असंतृप्त कार्बोक्जिलिक एसिड दोनों के अवशेष शामिल हो सकते हैं।
सामान्य परिस्थितियों में, असंतृप्त एसिड के अवशेष वाले वसा अक्सर तरल होते हैं। वे कहते हैं तेल. मूल रूप से, ये वनस्पति मूल के वसा हैं - अलसी, भांग, सूरजमुखी और अन्य तेल (ताड़ और नारियल तेल के अपवाद के साथ - सामान्य परिस्थितियों में ठोस)। मछली के तेल जैसे पशु मूल के तरल वसा कम आम हैं। सामान्य परिस्थितियों में पशु मूल के अधिकांश प्राकृतिक वसा ठोस (कम पिघलने वाले) पदार्थ होते हैं और इनमें मुख्य रूप से संतृप्त कार्बोक्जिलिक एसिड के अवशेष होते हैं, उदाहरण के लिए, मेमने की चर्बी।
वसा की संरचना उनके भौतिक और रासायनिक गुणों को निर्धारित करती है।
वसा के भौतिक गुण
वसा पानी में अघुलनशील होते हैं, उनका गलनांक स्पष्ट नहीं होता और पिघलने पर उनकी मात्रा काफी बढ़ जाती है।
वसा की समग्र अवस्था ठोस होती है, यह इस तथ्य के कारण है कि वसा में संतृप्त एसिड के अवशेष होते हैं और वसा के अणु सघन पैकिंग में सक्षम होते हैं। तेलों की संरचना में सीआईएस विन्यास में असंतृप्त एसिड के अवशेष शामिल हैं, इसलिए अणुओं की घनी पैकिंग असंभव है, और एकत्रीकरण की स्थिति तरल है।
वसा के रासायनिक गुण
वसा (तेल) एस्टर हैं और एस्टर प्रतिक्रियाओं की विशेषता रखते हैं।
यह स्पष्ट है कि असंतृप्त कार्बोक्जिलिक एसिड के अवशेष वाले वसा के लिए, असंतृप्त यौगिकों की सभी प्रतिक्रियाएं विशेषता हैं। वे ब्रोमीन पानी को रंगहीन कर देते हैं और अन्य अतिरिक्त प्रतिक्रियाओं में प्रवेश करते हैं। व्यावहारिक दृष्टि से सबसे महत्वपूर्ण प्रतिक्रिया वसा का हाइड्रोजनीकरण है। ठोस एस्टर तरल वसा के हाइड्रोजनीकरण द्वारा प्राप्त किए जाते हैं। यह वह प्रतिक्रिया है जो मार्जरीन के उत्पादन का आधार है - वनस्पति तेलों से एक ठोस वसा। परंपरागत रूप से, इस प्रक्रिया को प्रतिक्रिया समीकरण द्वारा वर्णित किया जा सकता है:

सभी वसा, अन्य एस्टर की तरह, हाइड्रोलिसिस से गुजरते हैं:

एस्टर का हाइड्रोलिसिस एक प्रतिवर्ती प्रतिक्रिया है। हाइड्रोलिसिस उत्पादों के निर्माण को सुनिश्चित करने के लिए, इसे क्षारीय वातावरण (क्षार या Na 2 CO 3 की उपस्थिति में) में किया जाता है। इन स्थितियों के तहत, वसा का हाइड्रोलिसिस विपरीत रूप से होता है और कार्बोक्जिलिक एसिड के लवण का निर्माण होता है, जिसे कहा जाता है। क्षारीय वातावरण में वसा कहलाती है वसा का साबुनीकरण.
जब वसा को साबुनीकृत किया जाता है, तो ग्लिसरीन और साबुन बनते हैं - उच्च कार्बोक्जिलिक एसिड के सोडियम और पोटेशियम लवण:
सैपोनिफिकेशन– वसा का क्षारीय जलअपघटन, साबुन का उत्पादन।

साबुन- उच्च संतृप्त कार्बोक्जिलिक एसिड (सोडियम साबुन - ठोस, पोटेशियम साबुन - तरल) के सोडियम (पोटेशियम) लवण का मिश्रण।
साबुन सर्फेक्टेंट (सर्फ़ेक्टेंट, डिटर्जेंट के रूप में संक्षिप्त) हैं। साबुन का डिटर्जेंट प्रभाव इस तथ्य के कारण होता है कि साबुन वसा का पायसीकरण करता है। साबुन प्रदूषकों के साथ मिसेल बनाते हैं (अपेक्षाकृत, ये विभिन्न समावेशन वाले वसा हैं)।
साबुन के अणु का लिपोफिलिक भाग संदूषक में घुल जाता है, और हाइड्रोफिलिक भाग मिसेल की सतह पर समाप्त हो जाता है। मिसेल्स को उसी तरह से चार्ज किया जाता है, इसलिए वे विकर्षित होते हैं, और प्रदूषक और पानी एक इमल्शन में बदल जाते हैं (व्यावहारिक रूप से, यह गंदा पानी है)।

साबुन पानी में भी होता है, जो क्षारीय वातावरण बनाता है।
साबुन का उपयोग कठोर और समुद्री जल में नहीं किया जा सकता, क्योंकि परिणामी कैल्शियम (मैग्नीशियम) स्टीयरेट पानी में अघुलनशील होते हैं।

नामपद्धति
एस्टर के नाम, हाइड्रोकार्बन रेडिकल ए और एसिड के नाम से प्राप्त होते हैं, जिसमें अंत में "-ओइक एसिड" के बजाय प्रत्यय "एट" का उपयोग किया जाता है (जैसा कि अकार्बनिक लवण के नाम में: सोडियम कार्बोनेट, क्रोमियम नाइट्रेट), उदाहरण के लिए:

(अणुओं के टुकड़े और नामों के संबंधित टुकड़े एक ही रंग में हाइलाइट किए गए हैं।)
एस्टर को आमतौर पर एसिड और अल्कोहल के बीच प्रतिक्रिया उत्पाद के रूप में माना जाता है; उदाहरण के लिए, ब्यूटाइल प्रोपियोनेट को प्रोपियोनिक एसिड और ब्यूटेनॉल के बीच प्रतिक्रिया के परिणाम के रूप में माना जा सकता है।
यदि प्रारंभिक एसिड का तुच्छ नाम उपयोग किया जाता है, तो यौगिक के नाम में "एस्टर" शब्द शामिल किया जाता है, उदाहरण के लिए, सी 3 एच 7 सीओओसी 5 एच 11 - ब्यूटिरिक एसिड का एमाइल एस्टर।
सजातीय श्रृंखला

संवयविता
एस्टर की विशेषता तीन प्रकार की समरूपता है:
1. कार्बन श्रृंखला का समावयवता, ब्यूटानोइक एसिड के साथ एसिड अवशेष पर शुरू होता है, अल्कोहल अवशेष पर - प्रोपाइल अल्कोहल के साथ, उदाहरण के लिए:
2. एस्टर समूह की स्थिति का समरूपता -सीओ-ओ-। इस प्रकार की समावयवता एस्टर से शुरू होती है जिनके अणुओं में कम से कम 4 कार्बन परमाणु होते हैं, उदाहरण के लिए:
3. इंटरक्लास आइसोमेरिज्म, एस्टर (एल्काइल एल्केनोएट्स) संतृप्त मोनोकारबॉक्सिलिक एसिड के लिए आइसोमेरिक हैं; उदाहरण के लिए:
असंतृप्त एसिड या असंतृप्त अल्कोहल वाले एस्टर के लिए, दो और प्रकार के आइसोमेरिज्म संभव हैं: एकाधिक बंधन की स्थिति का आइसोमेरिज्म; सीआईएस-ट्रांस आइसोमेरिज्म।
भौतिक गुण
एसिड और अल्कोहल के निचले समरूपों के एस्टर एक सुखद गंध के साथ रंगहीन, कम उबलते तरल पदार्थ होते हैं; खाद्य उत्पादों और सुगंध में सुगंधित योजक के रूप में उपयोग किया जाता है। एस्टर पानी में अच्छी तरह से नहीं घुलते हैं।
प्राप्ति के तरीके
1. प्राकृतिक उत्पादों से निकाला गया
2. ऐल्कोहॉल के साथ अम्लों की परस्पर क्रिया (एस्टरीफिकेशन प्रतिक्रियाएँ); उदाहरण के लिए:

रासायनिक गुण
1. एस्टर के लिए सबसे विशिष्ट प्रतिक्रियाएं अम्ल या क्षारीय हाइड्रोलिसिस (सैपोनिफिकेशन) हैं। ये ऐसी प्रतिक्रियाएं हैं जो एस्टरीफिकेशन प्रतिक्रियाओं के विपरीत हैं। उदाहरण के लिए:

2. जटिल ईथरों की कमी (हाइड्रोजनीकरण), जिसके परिणामस्वरूप अल्कोहल (एक या दो) बनते हैं; उदाहरण के लिए:

यदि प्रारंभिक एसिड पॉलीबेसिक है, तो या तो पूर्ण एस्टर का निर्माण संभव है - सभी एचओ समूहों को प्रतिस्थापित किया जाता है, या एसिड एस्टर - आंशिक प्रतिस्थापन। मोनोबैसिक एसिड के लिए, केवल पूर्ण एस्टर संभव हैं (चित्र 1)।
चावल। 1. एस्टर के उदाहरणअकार्बनिक और कार्बोक्जिलिक एसिड पर आधारित
एस्टर का नामकरण.
नाम निम्नानुसार बनाया गया है: सबसे पहले, एसिड से जुड़े समूह आर को इंगित किया जाता है, फिर प्रत्यय "एट" के साथ एसिड का नाम दर्शाया जाता है (जैसा कि अकार्बनिक लवण के नाम में: कार्बन परसोडियम नाइट्रेट परक्रोमियम). चित्र में उदाहरण. 2

चावल। 2. एस्टर के नाम. अणुओं के टुकड़े और नामों के संगत टुकड़े एक ही रंग में हाइलाइट किए जाते हैं। एस्टर को आमतौर पर एसिड और अल्कोहल के बीच प्रतिक्रिया उत्पादों के रूप में माना जाता है; उदाहरण के लिए, ब्यूटाइल प्रोपियोनेट को प्रोपियोनिक एसिड और ब्यूटेनॉल के बीच प्रतिक्रिया के परिणाम के रूप में माना जा सकता है।
यदि आप तुच्छ का उपयोग करते हैं ( सेमी. पदार्थों के तुच्छ नाम) प्रारंभिक एसिड का नाम, फिर यौगिक के नाम में "एस्टर" शब्द शामिल है, उदाहरण के लिए, सी 3 एच 7 सीओओसी 5 एच 11 - ब्यूटिरिक एसिड का एमाइल एस्टर।
एस्टर का वर्गीकरण और संरचना.
अध्ययन किए गए और व्यापक रूप से उपयोग किए जाने वाले एस्टर में से अधिकांश कार्बोक्जिलिक एसिड से प्राप्त यौगिक हैं। खनिज (अकार्बनिक) एसिड पर आधारित एस्टर इतने विविध नहीं हैं, क्योंकि खनिज अम्लों का वर्ग कार्बोक्जिलिक अम्लों की तुलना में कम है (यौगिकों की विविधता कार्बनिक रसायन विज्ञान की पहचान में से एक है)।
जब मूल कार्बोक्जिलिक एसिड और अल्कोहल में सी परमाणुओं की संख्या 6-8 से अधिक नहीं होती है, तो संबंधित एस्टर रंगहीन तैलीय तरल पदार्थ होते हैं, जिनमें अक्सर फल जैसी गंध होती है। वे फल एस्टर का एक समूह बनाते हैं। यदि एक सुगंधित अल्कोहल (एक सुगंधित नाभिक युक्त) एस्टर के निर्माण में शामिल होता है, तो ऐसे यौगिकों में, एक नियम के रूप में, फल की बजाय पुष्प गंध होती है। इस समूह के सभी यौगिक पानी में व्यावहारिक रूप से अघुलनशील हैं, लेकिन अधिकांश कार्बनिक सॉल्वैंट्स में आसानी से घुलनशील हैं। ये यौगिक अपनी सुखद सुगंधों की विस्तृत श्रृंखला के कारण दिलचस्प हैं (तालिका 1); उनमें से कुछ को पहले पौधों से अलग किया गया था और बाद में कृत्रिम रूप से संश्लेषित किया गया था।
| मेज़ 1. कुछ एस्टर, फल या फूलों की सुगंध वाला (यौगिक सूत्र और नाम में मूल अल्कोहल के टुकड़े बोल्ड में हाइलाइट किए गए हैं) | ||
| एस्टर फॉर्मूला | नाम | सुगंध |
| सीएच 3 सीओओ सी 4 एच 9 | ब्यूटाइलएसीटेट | नाशपाती |
| सी 3 एच 7 सीओओ सीएच 3 | मिथाइलब्यूटिरिक एसिड एस्टर | सेब |
| सी 3 एच 7 सीओओ सी 2 एच 5 | एथिलब्यूटिरिक एसिड एस्टर | अनानास |
| सी 4 एच 9 सीओओ सी 2 एच 5 | एथिल | गहरा लाल |
| सी 4 एच 9 सीओओ सी 5 एच 11 | आइसोएमिलआइसोवालेरिक एसिड एस्टर | केला |
| सीएच 3 सीओओ सीएच 2 सी 6 एच 5 | लोबानएसीटेट | चमेली |
| सी 6 एच 5 सीओओ सीएच 2 सी 6 एच 5 | लोबानबेंजोएट | फूलों |
जब एस्टर में शामिल कार्बनिक समूहों का आकार सी 15-30 तक बढ़ जाता है, तो यौगिक प्लास्टिक, आसानी से नरम होने वाले पदार्थों की स्थिरता प्राप्त कर लेते हैं। इस समूह को वैक्स कहा जाता है; वे आमतौर पर गंधहीन होते हैं। मोम में विभिन्न एस्टर का मिश्रण होता है; मोम के घटकों में से एक, जिसे अलग किया गया था और इसकी संरचना निर्धारित की गई थी, वह पामिटिक एसिड सी 15 एच 31 सीओओसी 31 एच 63 का माइरिसिल एस्टर है। चीनी मोम (कोचीनियल उत्सर्जन का एक उत्पाद - पूर्वी एशिया के कीड़े) में सेरोटिक एसिड सी 25 एच 51 सीओओसी 26 एच 53 का सेरिल एस्टर होता है। इसके अलावा, मोम में मुक्त कार्बोक्जिलिक एसिड और अल्कोहल भी होते हैं, जिनमें बड़े कार्बनिक समूह शामिल होते हैं। मोम पानी से गीला नहीं होता है और गैसोलीन, क्लोरोफॉर्म और बेंजीन में घुलनशील होता है।
तीसरा समूह वसा है। मोनोहाइड्रिक अल्कोहल आरओएच पर आधारित पिछले दो समूहों के विपरीत, सभी वसा ट्राइहाइड्रिक अल्कोहल ग्लिसरॉल एचओसीएच 2 - सीएच (ओएच) - सीएच 2 ओएच से बने एस्टर हैं। वसा बनाने वाले कार्बोक्जिलिक एसिड में आमतौर पर 9-19 कार्बन परमाणुओं के साथ एक हाइड्रोकार्बन श्रृंखला होती है। पशु वसा (गाय का मक्खन, भेड़ का बच्चा, चरबी) प्लास्टिक, गलने योग्य पदार्थ हैं। वनस्पति वसा (जैतून, बिनौला, सूरजमुखी तेल) चिपचिपे तरल पदार्थ हैं। पशु वसा में मुख्य रूप से स्टीयरिक और पामिटिक एसिड के ग्लिसराइड का मिश्रण होता है (चित्र 3ए, बी)। वनस्पति तेलों में थोड़ी कम कार्बन श्रृंखला लंबाई वाले एसिड के ग्लिसराइड होते हैं: लॉरिक सी 11 एच 23 सीओओएच और मिरिस्टिक सी 13 एच 27 सीओओएच। (स्टीयरिक और पामिटिक एसिड की तरह, ये संतृप्त एसिड हैं)। ऐसे तेलों को उनकी स्थिरता को बदले बिना लंबे समय तक हवा में संग्रहीत किया जा सकता है, और इसलिए उन्हें गैर-सुखाने वाला कहा जाता है। इसके विपरीत, अलसी के तेल में असंतृप्त लिनोलिक एसिड ग्लिसराइड होता है (चित्र 3बी)। जब सतह पर एक पतली परत में लगाया जाता है, तो ऐसा तेल दोहरे बंधन के साथ पोलीमराइजेशन के दौरान वायुमंडलीय ऑक्सीजन के प्रभाव में सूख जाता है, और एक लोचदार फिल्म बनती है जो पानी और कार्बनिक सॉल्वैंट्स में अघुलनशील होती है। प्राकृतिक सुखाने वाला तेल अलसी के तेल से बनाया जाता है।

चावल। 3. स्टीयरिक और पामिटिक एसिड के ग्लिसराइड (ए और बी)- पशु वसा के घटक. लिनोलिक एसिड ग्लिसराइड (बी) अलसी के तेल का एक घटक है।
खनिज एसिड के एस्टर (एल्काइल सल्फेट्स, एल्काइल बोरेट्स जिनमें कम अल्कोहल सी 1-8 के टुकड़े होते हैं) तैलीय तरल पदार्थ होते हैं, उच्च अल्कोहल के एस्टर (सी 9 से शुरू) ठोस यौगिक होते हैं।
एस्टर के रासायनिक गुण.
कार्बोक्जिलिक एसिड के एस्टर की सबसे विशेषता एस्टर बंधन का हाइड्रोलाइटिक (पानी के प्रभाव में) दरार है; एक तटस्थ वातावरण में यह धीरे-धीरे आगे बढ़ता है और एसिड या बेस की उपस्थिति में स्पष्ट रूप से तेज हो जाता है, क्योंकि एच + और एचओ - आयन इस प्रक्रिया को उत्प्रेरित करते हैं (चित्र 4ए), हाइड्रॉक्सिल आयन अधिक कुशलता से कार्य करते हैं। क्षार की उपस्थिति में जल-अपघटन को साबुनीकरण कहा जाता है। यदि आप गठित सभी एसिड को बेअसर करने के लिए पर्याप्त मात्रा में क्षार लेते हैं, तो एस्टर का पूर्ण साबुनीकरण होता है। यह प्रक्रिया औद्योगिक पैमाने पर की जाती है, और ग्लिसरॉल और उच्च कार्बोक्जिलिक एसिड (सी 15-19) क्षार धातु लवण के रूप में प्राप्त होते हैं, जो साबुन हैं (चित्र 4बी)। वनस्पति तेलों में मौजूद असंतृप्त अम्लों के टुकड़े, किसी भी असंतृप्त यौगिकों की तरह, हाइड्रोजनीकृत किए जा सकते हैं, हाइड्रोजन दोहरे बंधनों से जुड़ जाता है और पशु वसा के समान यौगिक बनते हैं (चित्र 4बी)। इस विधि का उपयोग करके, सूरजमुखी, सोयाबीन या मकई के तेल के आधार पर औद्योगिक रूप से ठोस वसा का उत्पादन किया जाता है। मार्जरीन प्राकृतिक पशु वसा और विभिन्न खाद्य योजकों के साथ मिश्रित वनस्पति तेलों के हाइड्रोजनीकरण उत्पादों से बनाया जाता है।

संश्लेषण की मुख्य विधि कार्बोक्जिलिक एसिड और अल्कोहल की परस्पर क्रिया है, जो एसिड द्वारा उत्प्रेरित होती है और पानी की रिहाई के साथ होती है। यह प्रतिक्रिया चित्र में दिखाई गई प्रतिक्रिया के विपरीत है। 3ए. प्रक्रिया को वांछित दिशा (एस्टर संश्लेषण) में आगे बढ़ाने के लिए, प्रतिक्रिया मिश्रण से पानी को आसुत (आसुत) किया जाता है। लेबल किए गए परमाणुओं का उपयोग करके विशेष अध्ययन के माध्यम से, यह स्थापित करना संभव था कि संश्लेषण प्रक्रिया के दौरान, ओ परमाणु, जो परिणामी पानी का हिस्सा है, एसिड से अलग होता है (लाल बिंदीदार फ्रेम के साथ चिह्नित), और अल्कोहल से नहीं ( अवास्तविक विकल्प को नीले बिंदीदार फ्रेम के साथ हाइलाइट किया गया है)।
उसी योजना का उपयोग करके, अकार्बनिक एसिड के एस्टर, उदाहरण के लिए, नाइट्रोग्लिसरीन, प्राप्त किए जाते हैं (छवि 5 बी)। एसिड के बजाय, एसिड क्लोराइड का उपयोग किया जा सकता है; यह विधि कार्बोक्जिलिक (छवि 5 सी) और अकार्बनिक एसिड (छवि 5 डी) दोनों के लिए लागू है।
आरसीएल हैलाइड्स के साथ कार्बोक्जिलिक एसिड लवण की परस्पर क्रिया से एस्टर भी बनते हैं (चित्र 5डी); प्रतिक्रिया सुविधाजनक है क्योंकि यह अपरिवर्तनीय है - जारी अकार्बनिक नमक अवक्षेप के रूप में कार्बनिक प्रतिक्रिया माध्यम से तुरंत हटा दिया जाता है।
एस्टर का उपयोग.
एथिल फॉर्मेट एचसीओओसी 2 एच 5 और एथिल एसीटेट एच 3 सीओओसी 2 एच 5 का उपयोग सेल्यूलोज वार्निश (नाइट्रोसेल्यूलोज और सेल्यूलोज एसीटेट पर आधारित) के लिए सॉल्वैंट्स के रूप में किया जाता है।
कम अल्कोहल और एसिड पर आधारित एस्टर (तालिका 1) का उपयोग खाद्य उद्योग में फलों का सार बनाने के लिए किया जाता है, और सुगंधित अल्कोहल पर आधारित एस्टर का उपयोग इत्र उद्योग में किया जाता है।
पॉलिश, स्नेहक, कागज (मोमयुक्त कागज) और चमड़े के लिए संसेचन रचनाएँ मोम से बनाई जाती हैं; इन्हें कॉस्मेटिक क्रीम और औषधीय मलहम में भी शामिल किया जाता है।
वसा, कार्बोहाइड्रेट और प्रोटीन के साथ मिलकर, पोषण के लिए आवश्यक खाद्य पदार्थों का एक समूह बनाते हैं; वे सभी पौधों और जानवरों की कोशिकाओं का हिस्सा होते हैं; इसके अलावा, जब वे शरीर में जमा होते हैं, तो वे ऊर्जा आरक्षित की भूमिका निभाते हैं। अपनी कम तापीय चालकता के कारण, वसा की परत जानवरों (विशेषकर समुद्री जानवरों - व्हेल या वालरस) को हाइपोथर्मिया से अच्छी तरह से बचाती है।
पशु और वनस्पति वसा उच्च कार्बोक्जिलिक एसिड, डिटर्जेंट और ग्लिसरॉल (छवि 4) के उत्पादन के लिए कच्चे माल हैं, जिनका उपयोग सौंदर्य प्रसाधन उद्योग में और विभिन्न स्नेहक के एक घटक के रूप में किया जाता है।
नाइट्रोग्लिसरीन (चित्र 4) एक प्रसिद्ध औषधि और विस्फोटक है, जो डायनामाइट का आधार है।
सुखाने वाले तेल वनस्पति तेलों से बनाए जाते हैं (चित्र 3), जो तेल पेंट का आधार बनते हैं।
सल्फ्यूरिक एसिड के एस्टर (चित्र 2) का उपयोग कार्बनिक संश्लेषण में एल्काइलेटिंग (एक यौगिक में एक एल्काइल समूह का परिचय) अभिकर्मकों के रूप में किया जाता है, और फॉस्फोरिक एसिड के एस्टर (चित्र 5) का उपयोग कीटनाशकों के साथ-साथ चिकनाई वाले तेलों में योजक के रूप में किया जाता है।
मिखाइल लेवित्स्की